第一张AI影像辅助决策三类医疗器械证 开启医疗人工智能商业化的新纪元
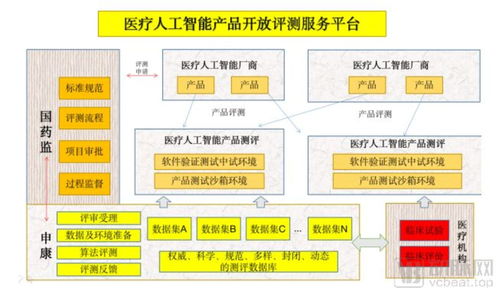
中国国家药品监督管理局(NMPA)颁发了国内首张用于影像辅助决策的人工智能(AI)软件的三类医疗器械注册证。这一里程碑事件,不仅仅是一张许可证的颁发,更是标志着中国医疗人工智能产业从研发、验证正式迈入规模化商业应用的新阶段,对整个行业具有深远的意义。
一、三类医疗器械证:医疗AI产品的“最高通行证”
在中国,医疗器械根据其风险等级分为一类、二类和三类,其中三类医疗器械是最高风险级别,通常用于支持或维持生命,或对人体具有潜在高风险,需进行严格的控制和管理。对于AI医疗软件而言,获得三类证意味着:
- 官方认可的安全性与有效性:该产品已经通过了最严格的临床验证和审评审批流程,其辅助诊断的准确性、稳定性和临床价值得到了监管机构和专家委员会的认可。
- 合法的市场准入资格:持证产品可以在医院等医疗机构内作为医疗器械正式销售、采购和使用,并可以纳入医保收费目录,实现了从“技术工具”到“医疗产品”的本质跨越。
- 明确的权责界定:作为获批的医疗器械,其使用过程中的责任主体得以明确,有助于推动AI在临床实践中的规范、可靠应用。
二、对“人工智能基础软件开发”行业的重大意义
这张证件的颁发,尤其对专注于医疗领域的人工智能基础软件开发公司,释放出多重积极信号:
- 明确了技术落地的合规路径:长期以来,AI医疗软件处于“技术先进但身份模糊”的境地。三类证审批路径的打通,为后续同类产品提供了清晰的注册申报范式和技术要求指南,极大地降低了企业的政策不确定性。
- 验证了商业模式的可行性:获证意味着产品可以产生直接的经济回报。这将吸引更多资本和人才进入该领域,推动从算法研究、数据标注、临床验证到注册申报的完整产业链走向成熟。
- 推动技术研发走向“深水区”:为了满足三类证的严苛要求,企业必须进行大规模、多中心的回顾性与前瞻性临床研究。这迫使AI开发从追求实验室的高精度指标,转向解决真实的、复杂的临床场景问题,如与不同品牌设备的适配、处理不完美的影像数据、提供可解释的决策依据等,从而驱动技术向更深、更实用方向发展。
- 加速医院端的采纳与融合:有了“官宣”背书,医院信息科、设备科和临床科室在引入AI产品时将更有据可依。这将加速AI与医院信息系统(HIS/PACS等)的深度集成,使其真正成为医生工作流中可信赖的一环,提升诊疗效率和均质化水平。
三、面临的挑战与未来展望
首证落地是起点,而非终点。行业在欢欣鼓舞的也需清醒认识到挑战:
- 高昂的获证成本与时间:三类证注册过程漫长(通常需数年),投入巨大,对初创企业是严峻考验。
- 持续监管与算法迭代:AI软件需要持续学习优化,但其作为医疗器械,任何核心算法的更新都可能需要重新报批,如何平衡监管的严肃性与技术的敏捷性是一大课题。
- 支付体系与价值认定:如何为AI辅助诊断服务制定合理的收费标准,并使其价值被医保和各方支付者广泛接受,是商业化成功的关键。
首张三类证如同一声发令枪,预示着中国AI医疗软件赛道将进入以“持证上岗”为标志的规范化、商业化竞速新阶段。它不仅是单个产品的胜利,更是为整个医疗人工智能基础软件开发行业照亮了前路——唯有将顶尖算法与严谨的医疗器械质量管理体系、扎实的临床证据深度融合,才能创造出经得起市场和生命检验的真正价值,最终实现人工智能赋能医疗健康事业的宏伟愿景。
如若转载,请注明出处:http://www.ywtdzjx.com/product/62.html
更新时间:2026-04-04 14:20:40